摘要:
mRNA或RNA结合蛋白(RBP)的功能障碍会导致细胞老化和与年龄相关的退行性疾病;然而,关于RBP介导的转录后调节影响细胞衰老和相关疾病过程的机制的信息是有限的。在这项研究中,发现PUM1与人间充质干细胞(MSC)的自我更新能力和衰老过程有关。PUM1与Toll样受体4(TLR4)的3'-非翻译区相互作用以抑制TLR4mRNA翻译并调节核因子-κB(NF-κB)的活性,NF-κB是MSCs衰老过程的主要调节因子。PUM1过表达保护MSCs免受H2O2-通过抑制TLR4介导的NF-κB活性诱导细胞衰老。TLR4介导的NF-κB活化是骨关节炎(OA)发病机制中的关键调节因子。即使在脂多糖(LPS)或白细胞介素-1β(IL-1β)等炎症诱导因子的影响下,PUM1过表达也增强了MSCs的软骨形成潜力,而在PUM1敲低介导的TLR4激活后,软骨形成潜力降低。PUM1水平在体外炎症条件下和人类和小鼠疾病模型的OA进展期间降低。人类软骨细胞中的PUM1敲低促进了软骨形成表型的丧失,而PUM1过表达保护细胞免受炎症介导的软骨形成表型破坏。使用编码小鼠PUM1的慢病毒载体的基因治疗显示出在OA小鼠模型中保持关节软骨完整性的前景。总之,PUM1是一种新型的MSC衰老抑制因子,而PUM1-TLR4调节轴代表了OA的潜在治疗靶点。

介绍
间充质干细胞(MSCs)具有作为再生受损组织的新型治疗选择的潜力。由于其自我更新和多能特性,MSCs可用于治疗多种疾病,尤其是骨关节炎(OA)和骨质疏松症等骨骼疾病。MSC用于肌肉骨骼疾病(包括骨骼和软骨疾病)的有希望的结果已得到证实。然而,MSCs体外扩增的继代培养与细胞衰老和自我更新有关,而MSCs体外长期培养会降低其多分化潜能,导致治疗潜力的丧失。因此,在分子水平上,与衰老相关的变化与OA的发展密切相关。已经表明,软骨组织中的软骨细胞密度随着年龄的增长而降低,并且衰老的软骨细胞中的细胞防御机制受损。在衰老过程中,软骨细胞产生细胞外基质蛋白的能力减弱。因此,了解MSCs和软骨细胞的衰老机制对于确定与年龄相关的疾病(如OA)的新治疗靶点至关重要。
mRNA或RNA结合蛋白(RBP)的失调与细胞衰老和年龄相关的退行性疾病有关;然而,人们对RBP介导的转录后调控如何影响这些过程知之甚少。人类基因组编码两种PUMILIO蛋白,PUMILIO1(PUM1)和PUMILIO2(PUM2),具有相似的RNA结合特异性。在小鼠中,具有Pum2突变的胚胎干细胞(ESCs)的自我更新和分化能力没有受损,而Pum2突变小鼠虽然睾丸较小,但仍能存活和繁殖。PUM1与神经变性和基因组稳定性调节有关。在一项研究中,Pum1或Pum2中的无效突变与身体和器官大小的剂量依赖性减小有关,并且删除这两个基因导致胚胎致死率,这意味着哺乳动物PUM1和PUM2可能与发育过程有关。然而,PUM1和PUM2在人MSCs和软骨细胞中的功能、靶点和调控机制仍不清楚。
在这里,本文旨在通过研究PUM1蛋白与Toll样受体4(TLR4)的3′-UTR的相互作用以及对核因子-κB(NF-κB)活性的影响来确定PUM1蛋白在细胞衰老和OA进展中的作用。在MSCs中,本文的研究结果可以帮助我们评估人类MSCs的自我更新能力和衰老过程,并让我们能够确定OA的潜在治疗靶点并防止细胞衰老。
方法与结果
通过体外和体内实验,体外实验结果显示:PUM1与MSC中的细胞衰老有关(见图一);PUM1靶向MSC中的TLR4(见图二);PUM1过表达保护MSC免受H2O2诱导的细胞衰老(见图三);体内实验结果进一步显示:PUM1在炎症微环境下保留MSC软骨形成潜力(见图四);PUM1表达的降低可能与OA发病机制有关(见图五);PUM1保护软骨细胞免受炎症反应,DNA损伤(NORAD)激活的非编码RNA似乎在骨关节炎中充当PUM1的上游调节剂(见图六);PUM1基因治疗可在小鼠OA模型中保持关节软骨的完整性(见图七)。
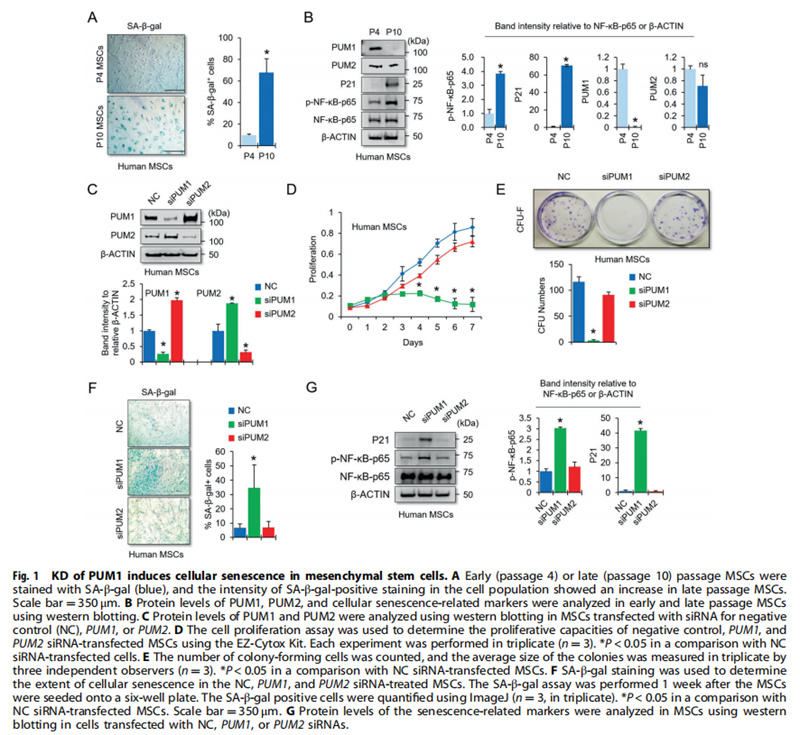
(图一)
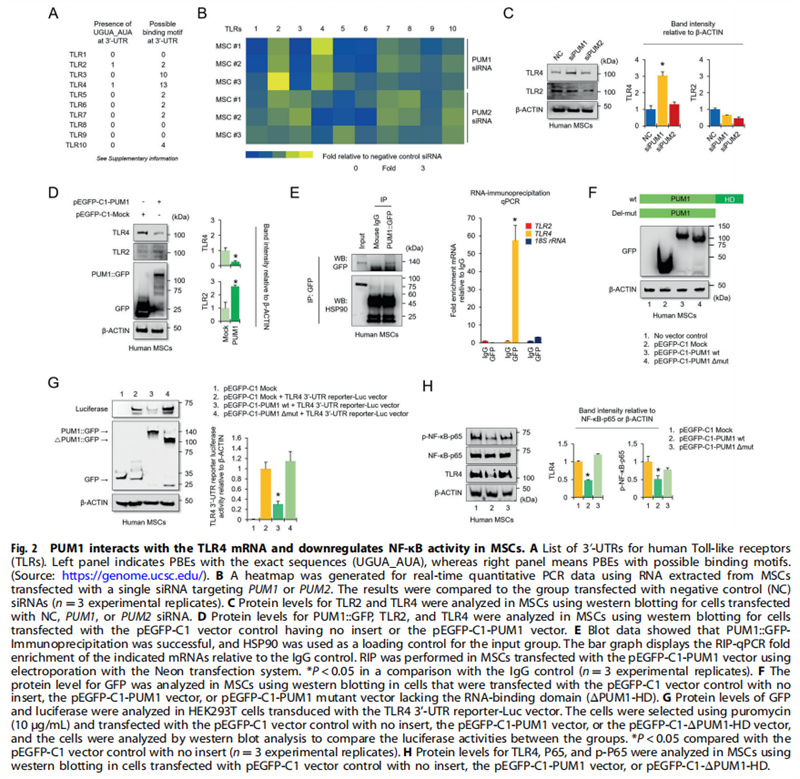
(图二)
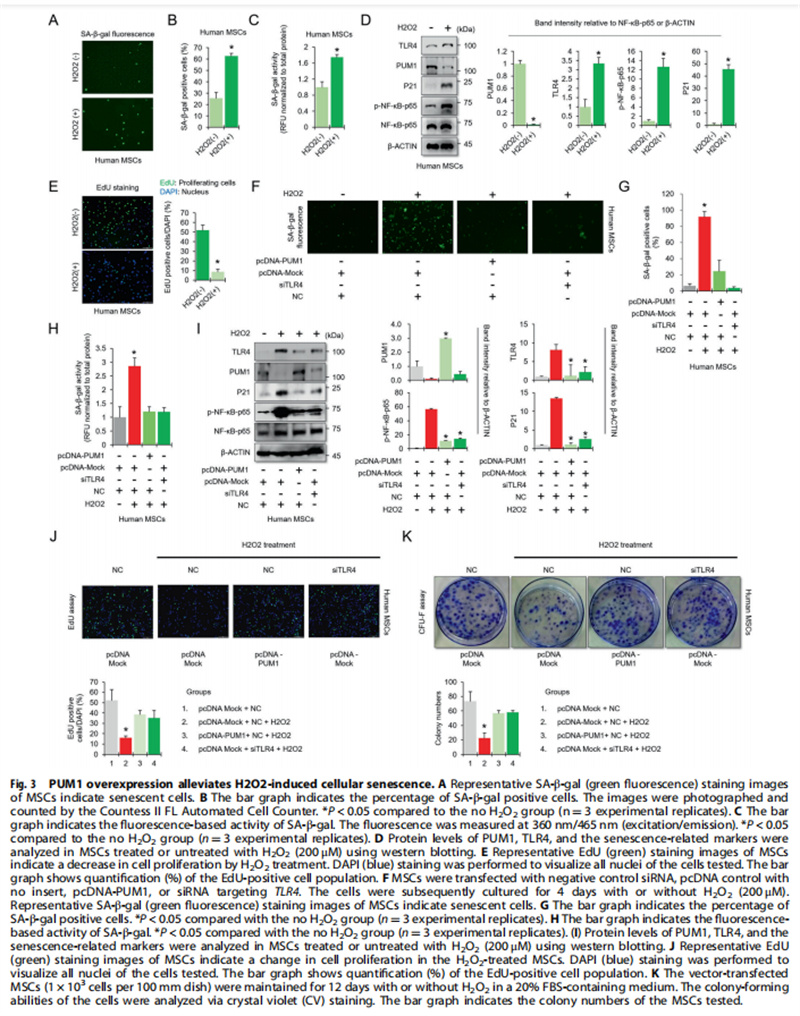
(图三)

(图四)
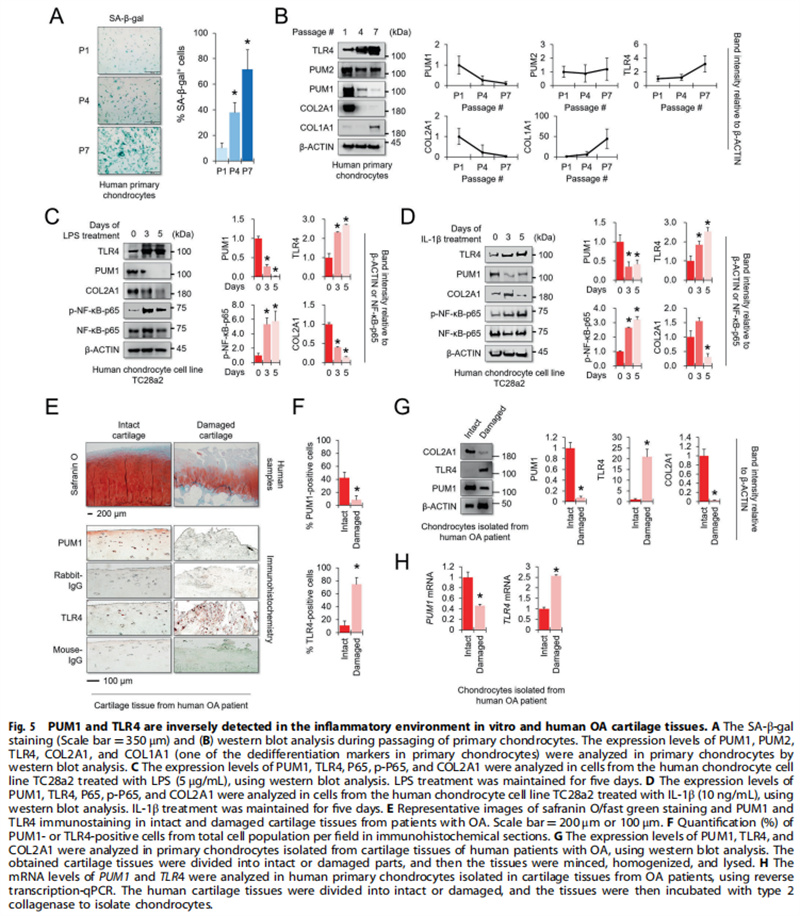
(图五)
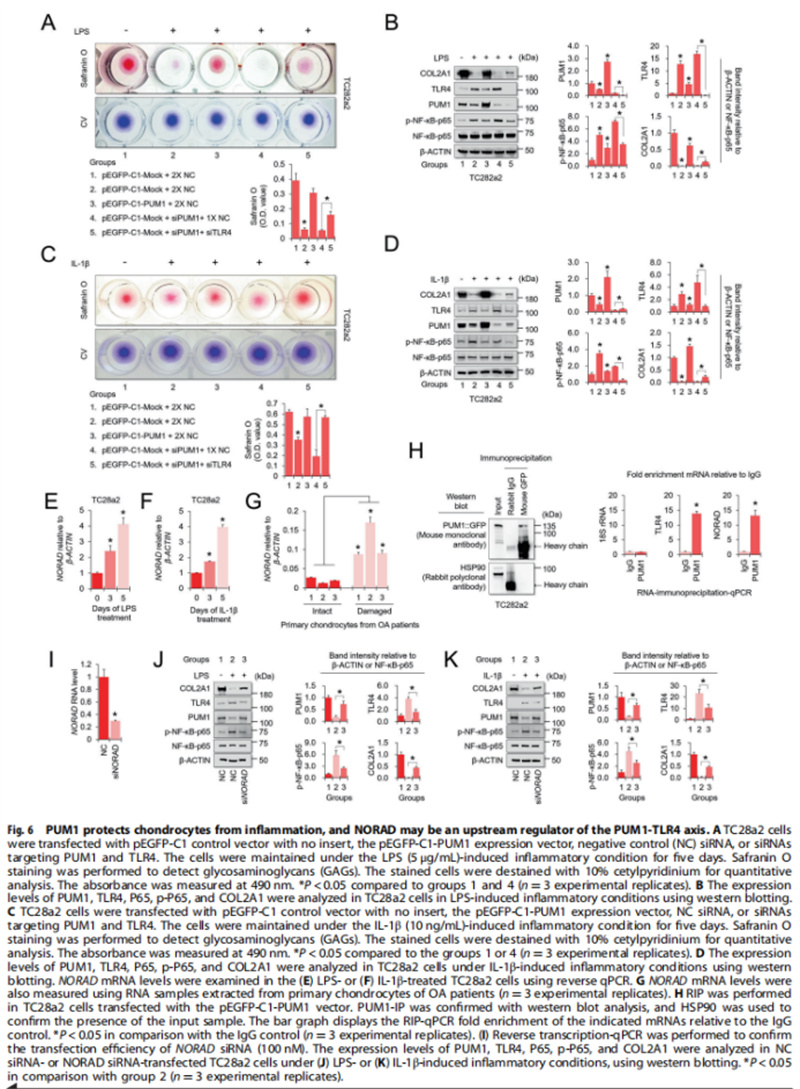
(图六)
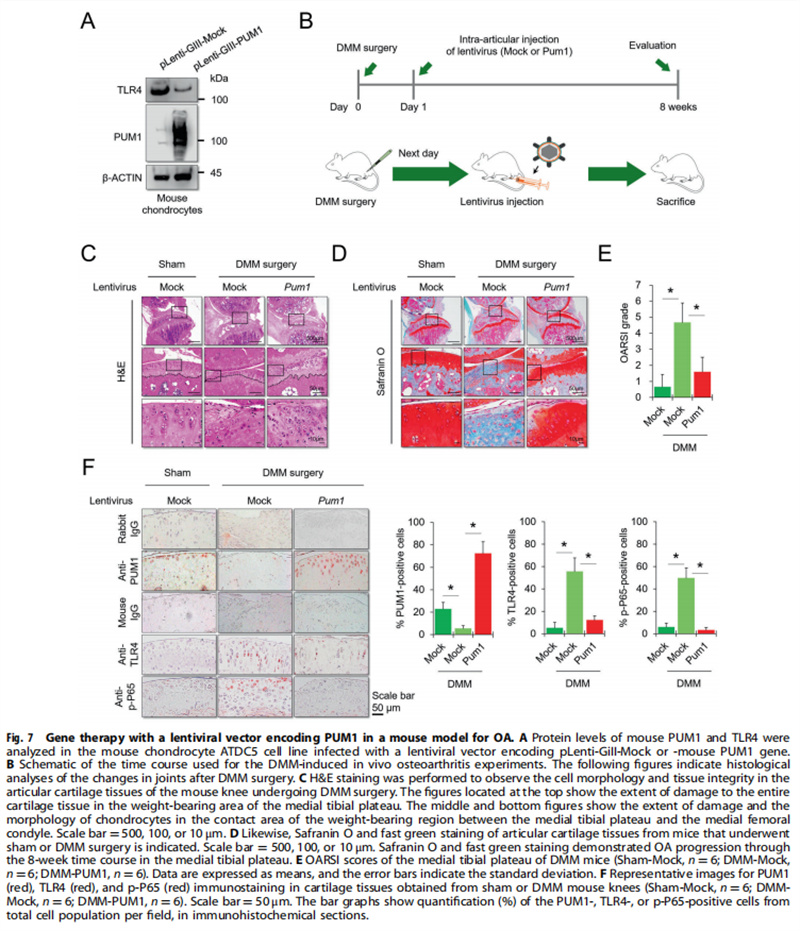
(图七)
结论
总体而言,在MSC衰老和OA发育过程中,PUM1表达下调,TLR4和NF-κB表达上调。本文证明了PUM1介导的TLR4-NF-κB信号转导的转录后抑制调节了TLR4的表达和PUM1与TLR43'-UTR的相互作用,导致NF-κB活性的下调。因此,诱导PUM1表达以减少TLR4-NF-κB在OA软骨中的炎症作用可能为治疗由TLR4-NF-κB信号传导引起的OA和年龄相关疾病提供一种新方法。总之,PUM1介导的TLR4表达调节有可能成为临床上适合OA治疗的靶点。因此,PUM1的关节内输送基因可能是一种有前途的预防OA进展的治疗方法。
文章出自:细胞实验外包 想了解更多请关注:http://www.do-gene.com




