摘要:
骨质疏松症(OP)的特征是骨小梁体积减少和髓腔微结构退化。尿石素A(UA)是一种由肠道微生物群产生的生物活性代谢物。UA是可测量的产物,被认为是最相关的尿石素,是多酚化合物的最终代谢产物.考虑到肠道微生物群介导的分解代谢作用与病理性骨病密切相关,探索UA减轻OP的生物学影响和分子机制至关重要。我们的研究旨在调查在雌激素缺乏引起的骨质流失的情况下,UA给药对OP进展的影响。体内结果表明,UA有效地减少了卵巢切除术引起的全身性骨质流失。在体外,UA以浓度依赖性方式抑制核因子-κB配体(RANKL)触发的破骨细胞生成的受体激活剂。信号转导研究和测序分析表明,UA显着降低了破骨细胞中炎性细胞因子(例如,IL-6和TNF-α)的表达。此外,细胞焦亡标志物(NLRP3、GSDMD和caspase-1)。与这一发现一致,使用NLRP3炎症小体抑制剂(MCC950)来治疗OP,发现调节细胞焦亡可以改善去势(OVX))小鼠的破骨细胞生成和骨质流失,这表明UA通过调节炎症信号依赖来抑制破骨细胞的形成焦亡途径。可以想象,UA给药可能是一种安全且有前景的治疗破骨细胞相关骨病(如OP)的策略。

介绍
骨质疏松症(OP)是老龄化人群中最常见的骨科代谢疾病,其特点是骨小梁体积进行性减少,导致骨骼结构脆弱,运动耐量低。最近,雌激素剥夺被认为是绝经后妇女OP的主要发病机制。骨骼中的扰动主要由成骨细胞骨形成和破骨细胞骨吸收之间的不协调活动协调。在生理条件下,破骨细胞的活性受到主要由成骨细胞分泌的细胞因子核因子-κB配体受体激活剂(RANKL)的精确调控。在骨重建过程中,骨吸收速度超过骨形成速度,导致骨量减少和脆性骨折。已经认识到在脊椎动物骨骼的破坏性条件下发生过度破骨细胞活化的病理学参与。因此,抑制破骨细胞介导的骨吸收是治疗骨质减少和OP最有希望的方案。
尿石素A(UA)是一种由石榴和坚果的肠道菌群产生的化合物,已被发现具有促进细胞功能的有益作用。在通过肠道菌群产生的代谢物中,UA作为一种具有有益作用的强效药理剂引起了相当多的关注。UA在对氧化应激和线粒体反应的细胞保护反应中发挥积极作用。然而,其在绝经后OP中的保护作用和确切机制尚不清楚。越来越多的证据表明,肠道菌群的代谢调节高度参与骨稳态。因此,本研究有意关注UA在OP小鼠模型中的生物学作用及其影响破骨细胞的作用和机制。
在这项研究中,在体内和体外评估了UA对绝经后OP的具体作用和分子机制。作者发现UA通过抑制RANKL触发的破骨细胞形成来改善雌激素缺乏诱导的OP小鼠模型中的OP。此外,测序分析显示,UA的给药显着降低了炎症因子的表达,并抑制了核苷酸结合寡聚化结构域(NOD)样受体介导的细胞焦亡信号通路。顺便说一下,经观察表明,抑制NOD样受体家族pyrin含有结构域的3(NLRP3)是介导细胞焦亡的关键靶点,可以减少去卵巢(OVX)小鼠的破骨细胞生成和骨质流失,表明UA通过抑制炎症信号依赖性细胞焦亡途径来抑制破骨细胞生成。总的来说,本研究结果表明,UA是治疗绝经后OP患者的一种有前景的策略,并且调节细胞焦亡级联反应可能是控制OP发病机制的新治疗策略。
方法与结果
本研究通过卵巢切除术建立了小鼠OP模型,然后用UA治疗OVX小鼠。实验结果显示,UA减少了小鼠卵巢切除术引起的骨质流失(见图一、图二)。作者通过在体外进行了各种细胞干预试验,研究结果表明,UA在体外抑制破骨细胞分化和肌动蛋白带形成(见图三)。为了进一步阐明UA抑制破骨细胞功能的具体机制,在有或没有UA(10 μM)处理的RAW264.7细胞中进行了全转录组RNAseq。两组细胞均用50 μM RANKL处理。研究结果进一步表明,UA抑制促炎细胞因子基因表达和巨噬细胞极化(见图四);UA通过炎症激活的NF-κB通路抑制破骨细胞焦亡(见图五)。考虑到NLRP3炎症小体是导致细胞焦亡的关键因素,作者推测靶向该寡聚体可能构成绝经后OP的潜在治疗方法,选择了MCC950(一种强效的NLRP3抑制剂)并确定了这种小分子的影响。实验结果显示,NLRP3炎症小体抑制缓解破骨细胞生成和雌激素缺乏诱导的OP(见图六)。
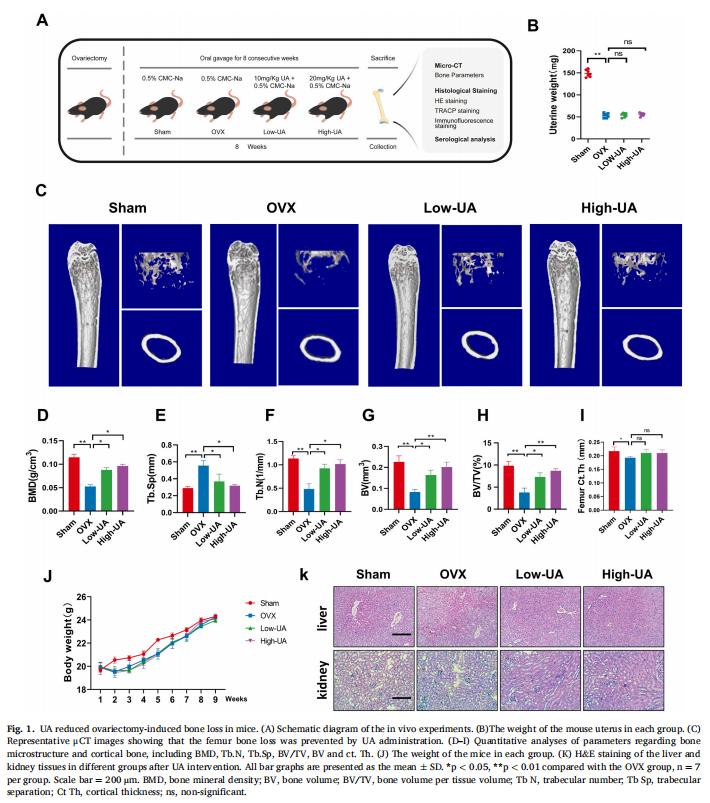
(图一)
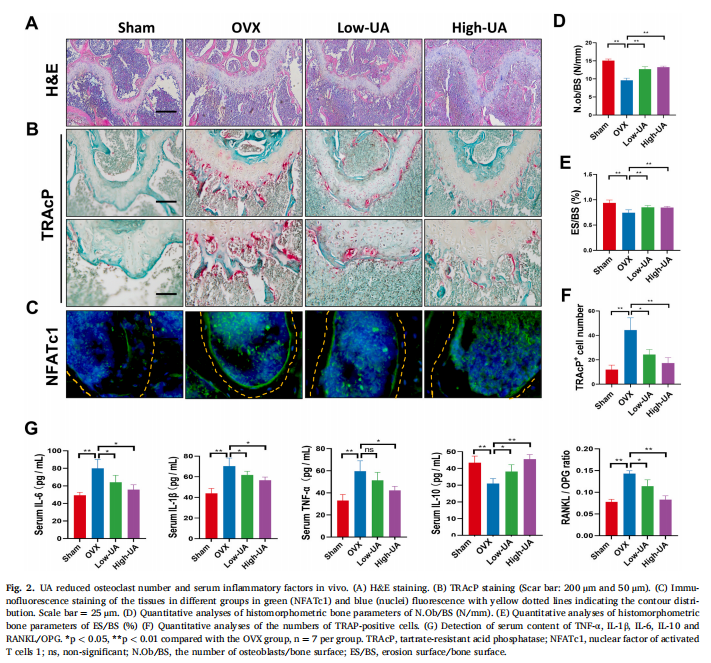
(图二)
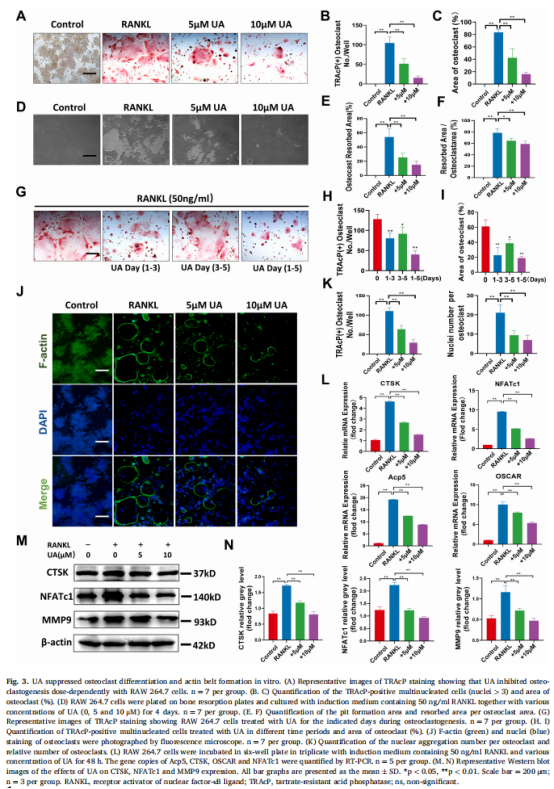
(图三)
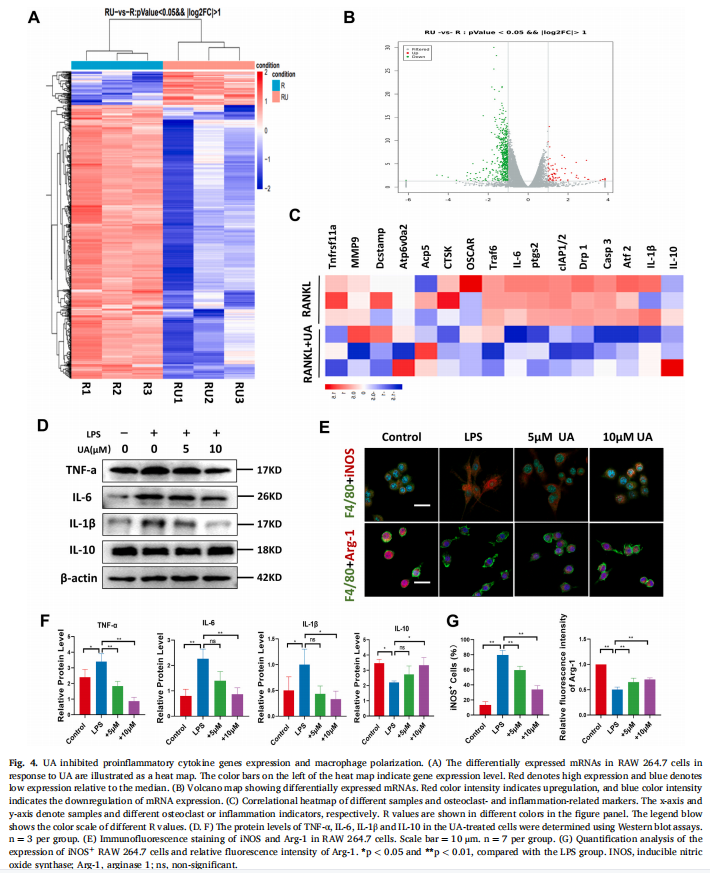
(图四)
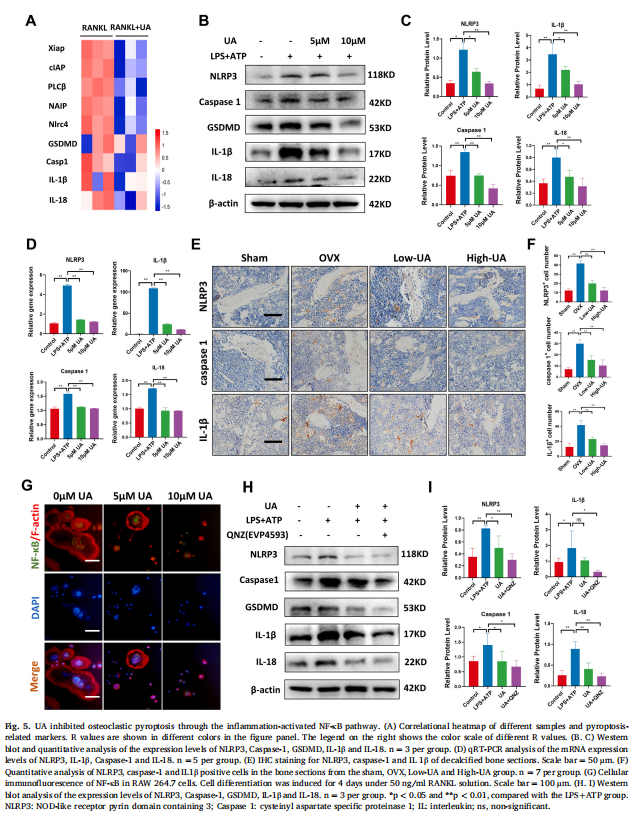
(图五)
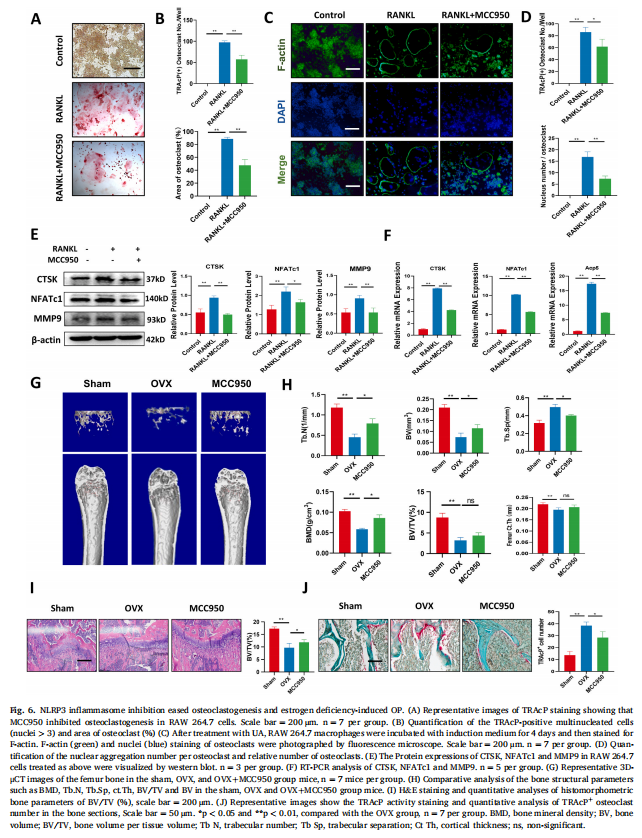
(图六)
结论
OP的特点是骨量低,是一种进行性多因素骨科疾病,会导致老年人肌肉力量下降和骨折风险增加。衰老和雌激素缺乏的影响被认为是绝经后妇女OP发病机制中最经久不衰的理论。除了这些原因,低钙摄入和不良免疫事件也可能导致骨组织的微观结构退化。确定新的临床药物始终是改善OP治疗的必要条件。破骨细胞和成骨细胞是通过其耦合活动参与骨代谢调节的两种主要细胞类型。破骨细胞是巨大的多核细胞,参与骨吸收过程,被认为是预防OP的主要目标。因此,可以采用抑制进行性破骨细胞过度活跃作为一种有效的治疗策略。
UA作为ET和EA的肠道微生物代谢物发挥作用。越来越多的证据表明,肠道微生物群的代谢调节与骨稳态高度相关。UA是肠道菌群的代谢产物,值得进一步研究。在本研究中,作者发现UA在体内阻止卵巢切除术诱导的OP的进展。在体外,在用50 ng/ml RANKL刺激后,破骨细胞活性被UA处理以浓度依赖性方式大大抑制,从而导致随后NFATc1表达的减弱,这与Weske的工作一致。
总之,本研究的结果表明,UA是肠道微生物群的一种代谢物,通过抑制破骨细胞的形成来改善卵巢切除术引起的骨质流失。从机制上讲,体外结果显示UA调节巨噬细胞极化并减轻炎症反应。此外,炎症因子的减弱表达阻止了NF-κB的核易位,从而抑制了NLRP3炎症小体触发的细胞焦亡级联反应。更有希望的是,抑制NLRP3炎症小体还可以防止体内OVX小鼠的广泛骨丢失,这意味着调节破骨细胞焦亡可能是一种抑制OP的新治疗策略发病。可以想象,UA给药可能是一种安全且有前景的治疗破骨细胞相关骨病(如OP)的策略。
文章出自:细胞实验 想了解更多请关注:http://www.do-gene.com




