
背景
不受控制的T细胞激活免疫反应在系统性硬化症(SSc)的发病机制中起关键作用,这种疾病的特点是全身性纤维化,特别是影响肺和皮肤。共刺激分子是免疫激活过程中的关键分子,最近的证据支持CD28和ICOS在纤维化发展中的作用。我们在此研究了双重ICOS/CD28拮抗剂acazicolcept (ALPN-101)在两个互补的SSc相关小鼠模型中的功效,这些模型概括了皮肤纤维化、间质性肺病和肺动脉高压。
方法与结果
在SSc患者中研究了循环可溶性ICOS和皮肤表达ICOS的表达。此后,在次氯酸(HOCL)诱导的皮肤纤维化小鼠模型和Fra-2转基因(Tg)小鼠模型中评估了阿齐考西普。在每个模型中,小鼠每周两次接受400 μg acazicolcept 或摩尔匹配剂量的Fc对照蛋白,持续6周。6周后,对皮肤和肺进行了评估。研究结果显示:与来自健康对照的样本相比,来自SSc患者的血清和SSc皮肤活检中的ICOS显着增加(见图一)。在HOCL和Fra-2 Tg小鼠中,在Fc对照组和阿齐考西普组之间观察到类似的体重变化,表明对阿齐考西普治疗具有良好的耐受性。在用HOCL攻击的小鼠中,acazicolcept诱导皮肤厚度、胶原蛋白含量、肌成纤维细胞数量(见图二)和以B细胞、T细胞、中性粒细胞和巨噬细胞为特征的炎症浸润显着降低(见图三)。在Fra-2 Tg小鼠模型中,acazicolcept治疗降低了肺胶原蛋白含量、纤维状胶原蛋白、组织学纤维化评分和右心室收缩压(RVSP)。与Fc对照处理的Fra-2 Tg小鼠相比,观察到阿齐考西普处理的Fra-2 Tg小鼠的CD4+和T效应记忆细胞的频率降低以及CD4+ T幼稚细胞百分比增加(见图四)。此外,acazicolcept降低了来自脾脏和肺的CD4+ T细胞上的CD69和PD-1表达(见图五)。acazicolcept 的目标参与通过阻断CD28和通过流式细胞术在治疗小鼠中检测ICOS来证明(见图六)。
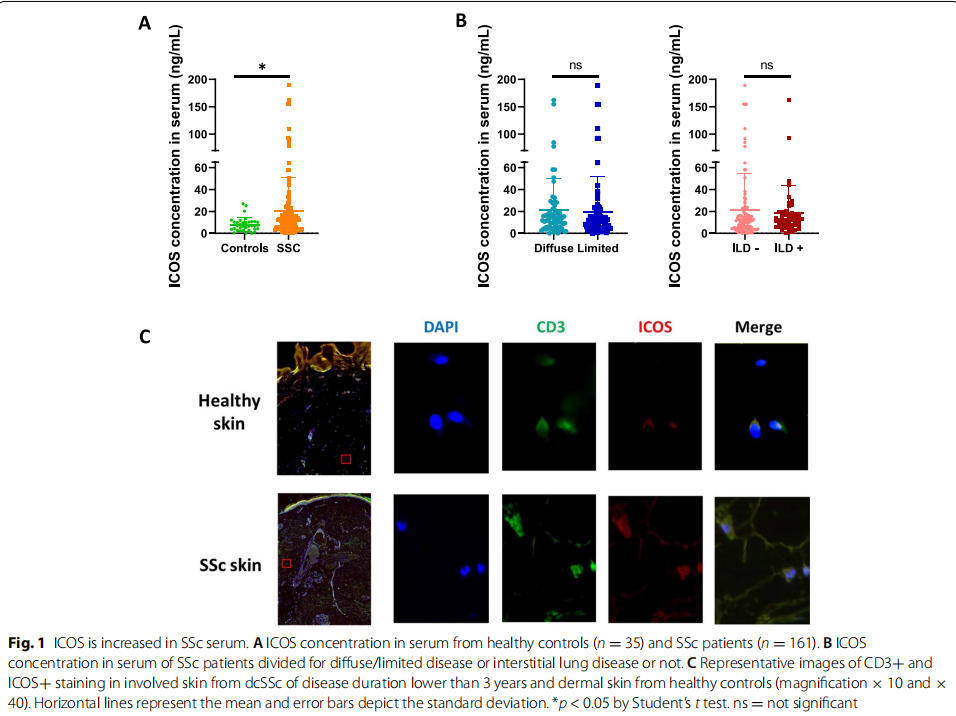
(图一)
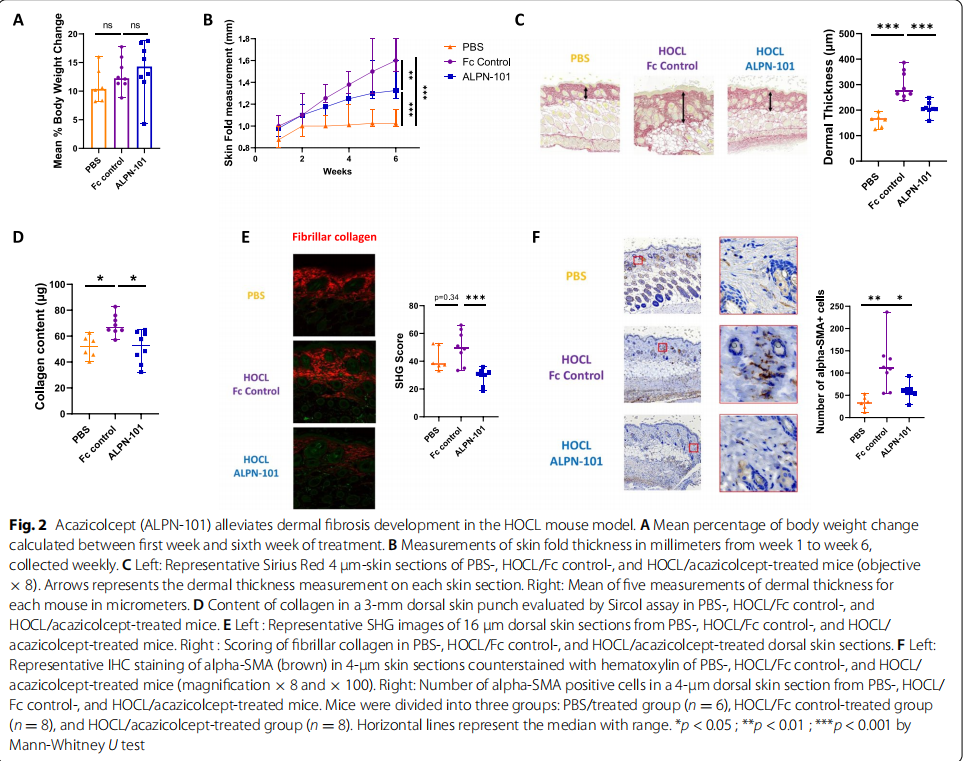
(图二)
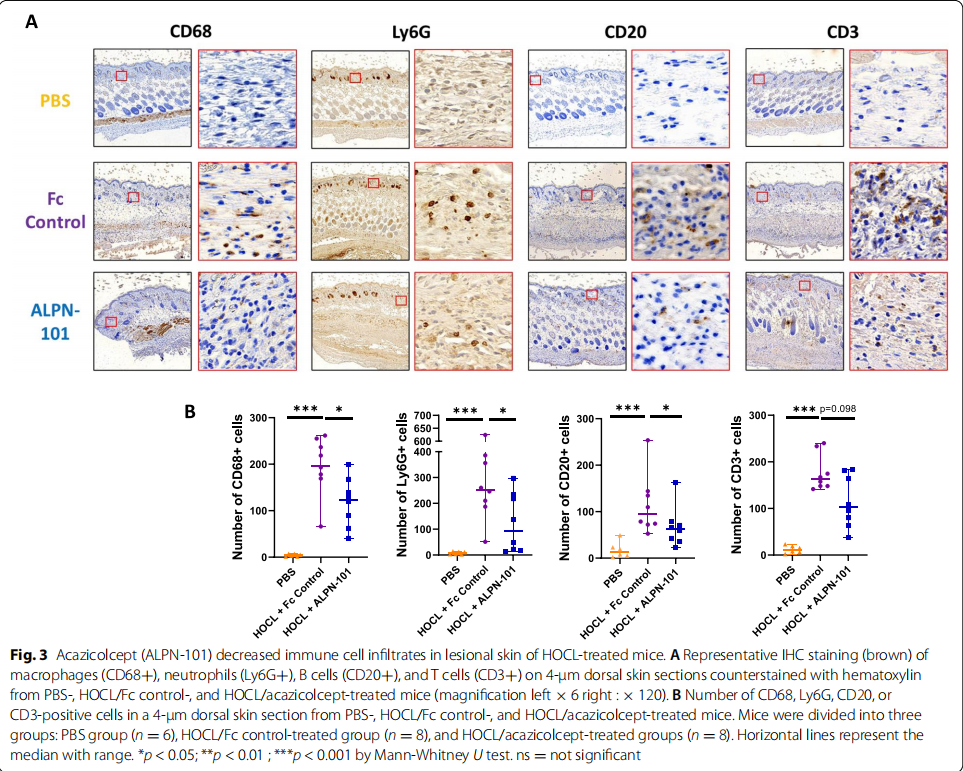
(图三)
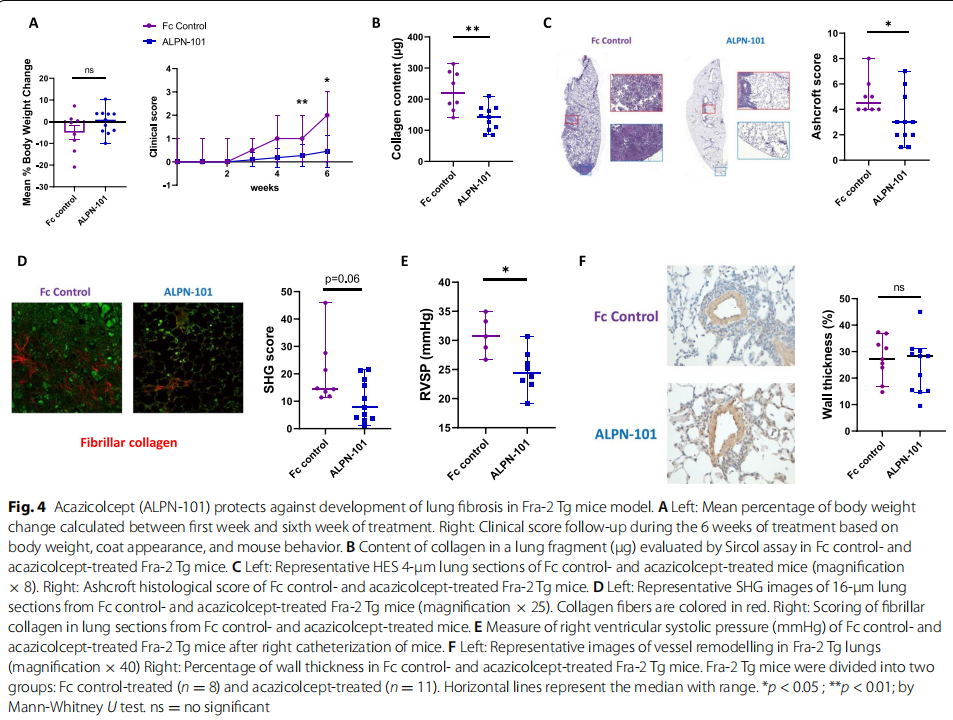
(图四)
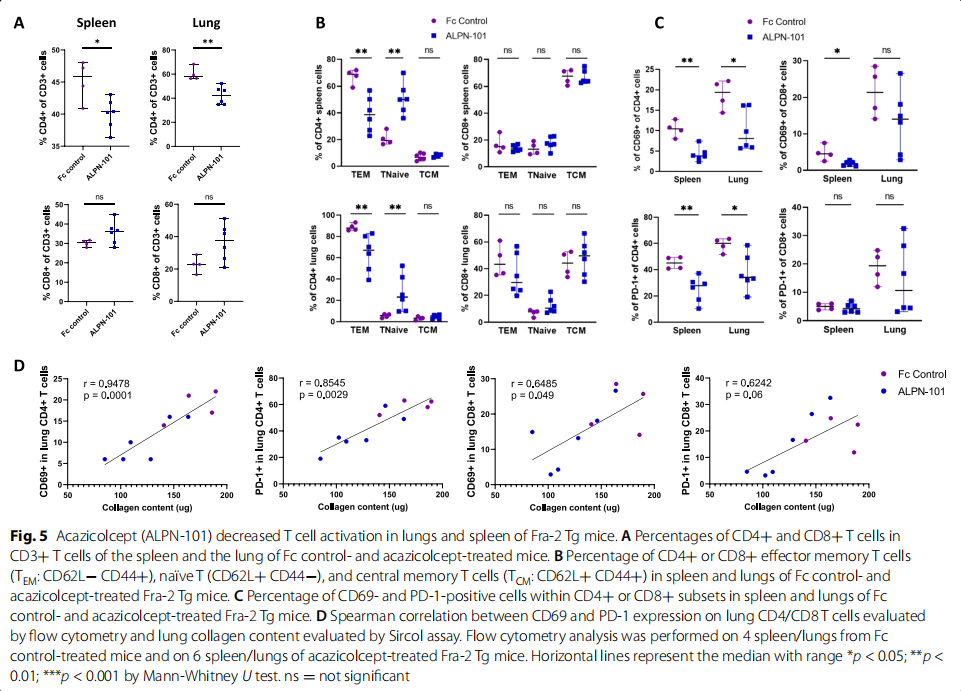
(图五)
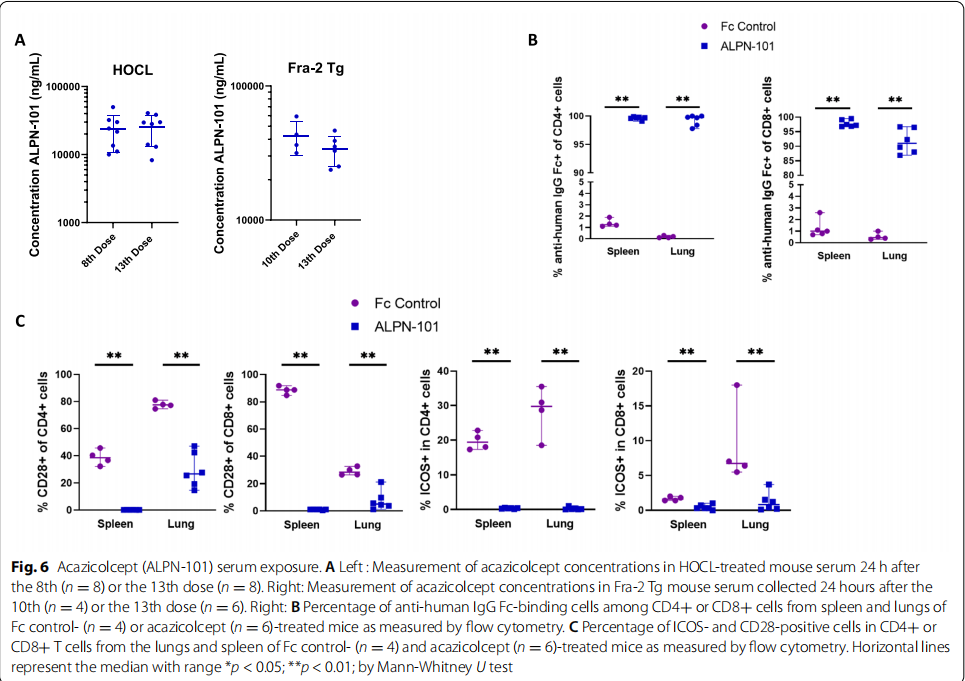
(图六)
本研究的实验结果证实了共刺激分子在炎症驱动的纤维化中的重要性。我们的数据突出了ICOS和CD28在SSc中的关键作用。使用互补模型,作者证明了acazicolcept的双重ICOS/CD28阻断减少了皮肤和肺纤维化并减轻了肺动脉高压。这些结果为后续ICOS/CD28靶向治疗的研究铺平了道路。
文章出自:动物实验外包 想了解更多请关注:http://www.do-gene.com/




