简单总结:
许多癌症类型的淋巴管生成受体Neuropilin-2(Nrp2)高表达,包括结肠直肠癌(CRC)。Nrp2被证明与CRC患者的体内肿瘤进展和不良预后相关。虽清楚。在这里,作者使用小鼠结直肠癌肿瘤来源的间充质样类器官来诱导Nrp2的消耗。我们证明,CRC类器官中Nrp2的缺失导致了表型的显著改变,其特征是间充质向上皮转化(MET),以及对IR信号和自噬的获得性依赖。这种表型保留在由CRC类器官产生的皮下肿瘤中。本文的结论是,在侵袭性结直肠癌中,Nrp2和替代的促生存机制之间存在着复杂的相互作用,这可以用于治疗。
摘要:
神经pilin-2(Nrp2)是淋巴管生成和淋巴转移的重要调节因子,与结直肠癌(CRC)的进展有关。然而,Nrp2在癌症进展中的肿瘤细胞内在作用尚不完全清楚。为了解决这个问题,作者使用CRISPR-Cas9技术,从具有间充质表型的小鼠CRC肿瘤中生成nrp2敲除类器官。转录组分析和肿瘤组织分析显示,Nrp2的缺失导致了间充质向上皮细胞的转化(MET),并伴随着极性的恢复和紧密连接的稳定。信号通路分析显示,nrp2敲除的类器官获得了重新依赖于胰岛素受体(IR)的信号通路和自噬作为替代生存机制。联合抑制IR信号通路和自噬可以抑制细胞-细胞连接的稳定,降低代谢活性,并导致nrp2敲除类器官的严重细胞死亡。综上所述,这些数据表明Nrp2在维持肿瘤源性结直肠癌类器官的侵袭性表型和生存方面发挥了关键作用。Nrp2、胰岛素受体信号转导和自噬之间的联系可能指导侵袭性结直肠癌的新的联合治疗策略的发展。

简介
由于远处转移的发展,结直肠癌(CRC)具有相当高的死亡率。25-50%的CRC患者发生结直肠肝转移(CRLM)。尽管外科手术和全身治疗取得了进展,但治疗效果和患者预后仍然很差。CRC是一种异质性疾病,可根据基因表达谱分为四种不同的共有分子亚型(CMS),反映特定信号通路激活的显着差异。CMS4亚型的特点是反映上皮间质转化(EMT)、转化生长因子(TGF)-β信号传导和高基质细胞含量的基因的高表达。CMS4与显着更差的无病生存期和总生存期相关。
尽管越来越多的证据表明肿瘤Nrp2与CRC进展相关,但Nrp2介导的结直肠癌生长和转移的机制仍然难以捉摸。为了研究Nrp2在侵袭性CRC中的肿瘤细胞内在作用,作者旨在生成一个与临床相关的、高EMT/富含基质的CMS4亚型非常相似的CRC模型。最近开发的三维(3D)类器官培养技术允许保留恶性细胞的遗传异质性和表型特征,如在初始癌组织中一样。本研究使用Notch1激活/p53缺失的肿瘤来产生间充质样CRC类器官。肿瘤概括了侵袭性人类CRC的间充质/EMT样表型,并且是从通过条件激活Notch1受体和消化上皮中的p53缺失产生的自发转移转基因小鼠模型中获得的。使用CRISPR-Cas9技术生成的类器官用于建立一种新的Nrp2表达耗尽的CRC类器官模型。在体外3D和体内皮下肿瘤发生模型中使用Nrp2敲除(Nrp2-/-)间充质样CRC类器官来探索Nrp2的癌细胞内在促肿瘤发生作用的潜在机制。
方法与结果
本研究利用小鼠间充质样CRC类器官诱导CRISPR-Cas9介导的Nrp2敲除。实验结果显示,小鼠CRC类器官中的Nrp2敲除诱导紧密连接稳定和EMT减少(见图一、图二);小鼠CRC类器官中的Nrp2敲除降低成人肠道干细胞基因表达而不影响胎儿肠道干细胞特征(见图三);小鼠CRC类器官中的Nrp2敲除诱导胰岛素受体信号上调(见图四);小鼠CRC类器官中的Nrp2消耗激活自噬(见图五);IR信号传导和早期自噬的联合抑制降低了Nrp2-/-CRC类器官的活力(见图六、图七);Nrp2表达与人类CRC的间充质分子亚型相关,并与自噬标志物表达负相关(见图八)。
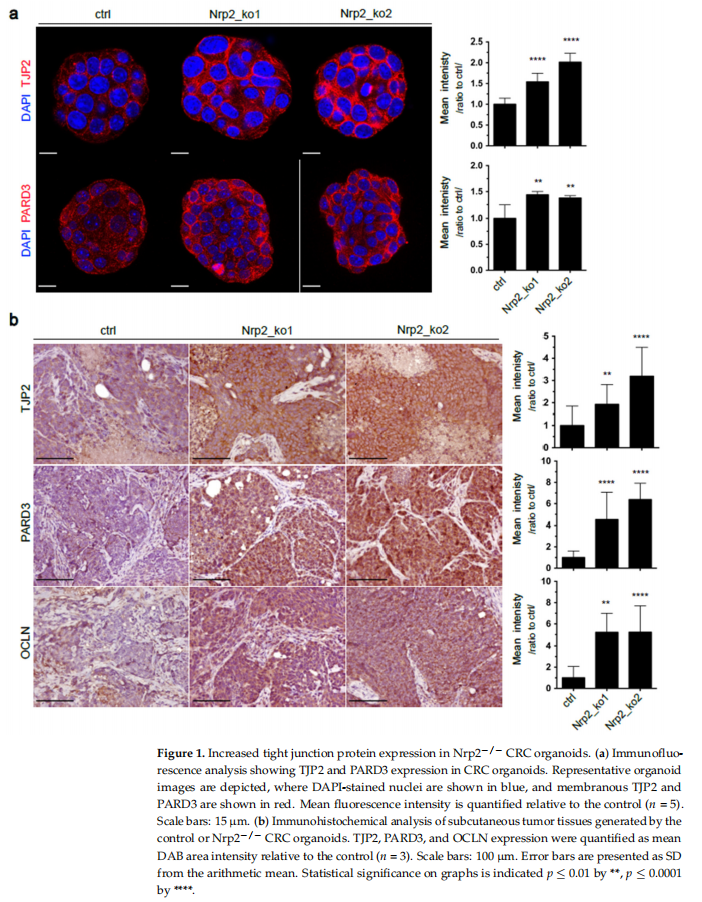
(图一)
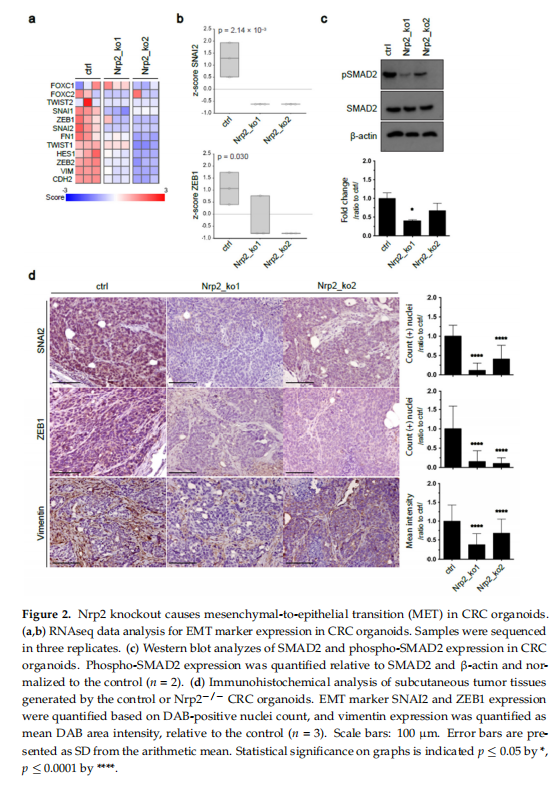
(图二)
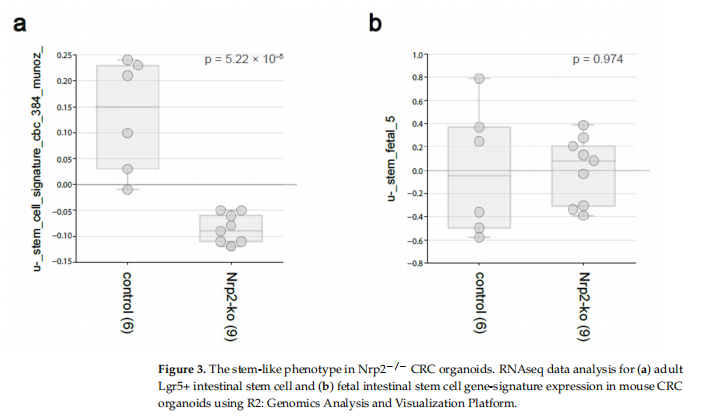
(图三)
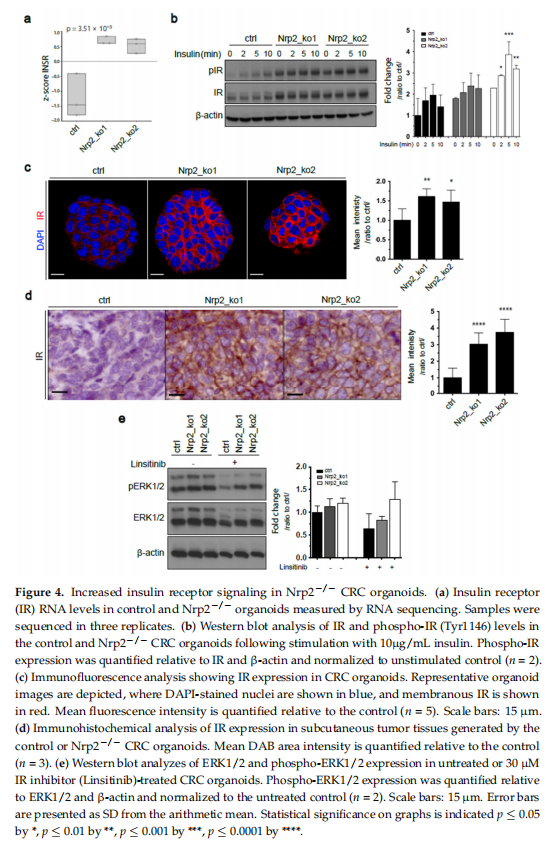
(图四)
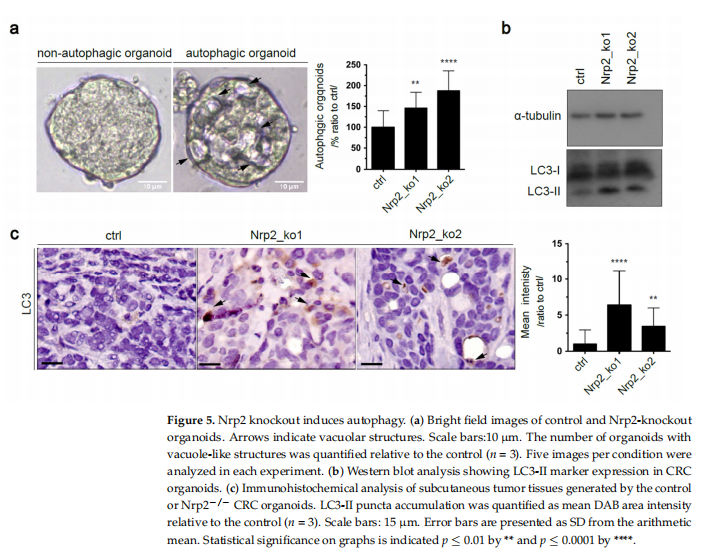
(图五)
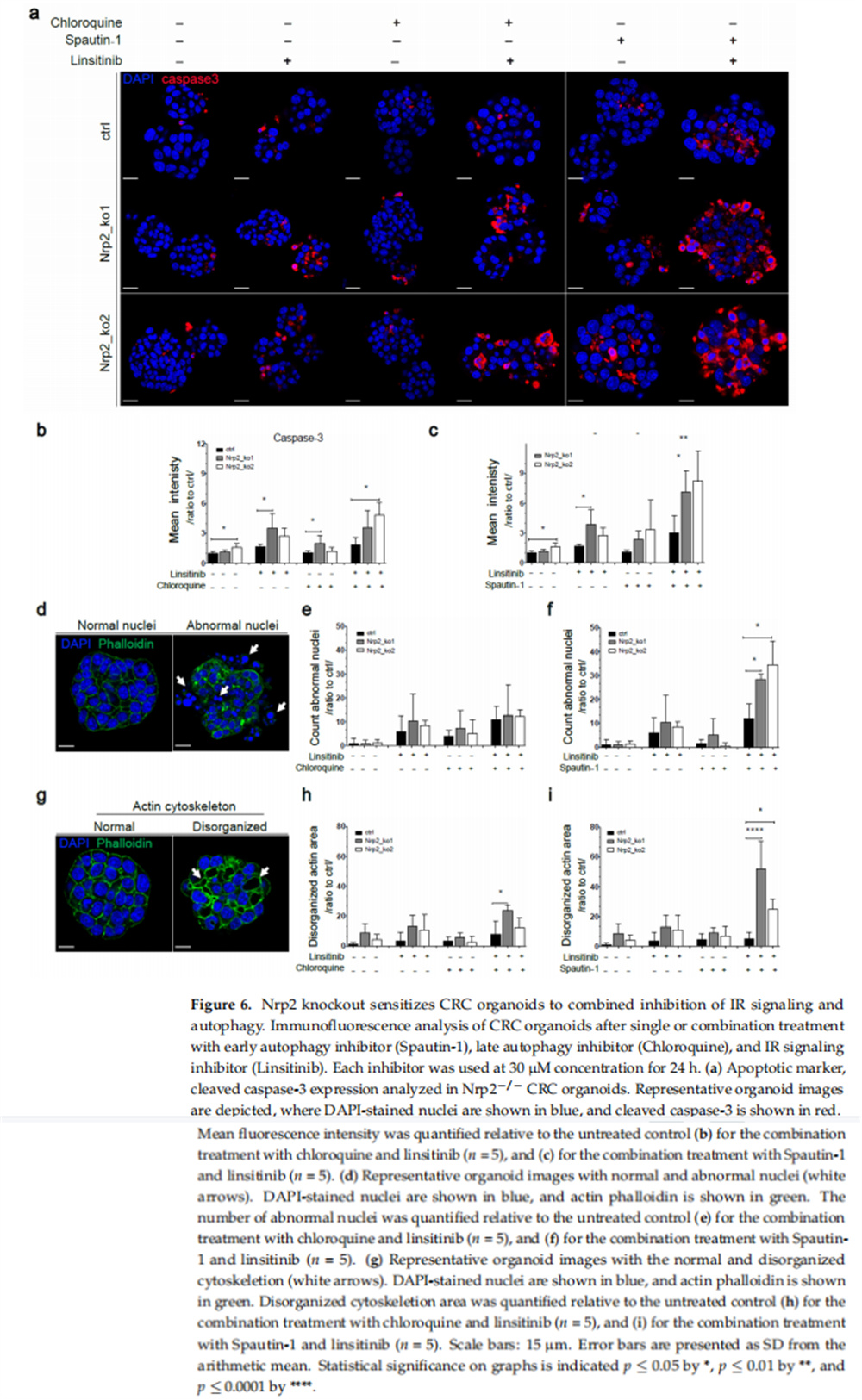
(图六)
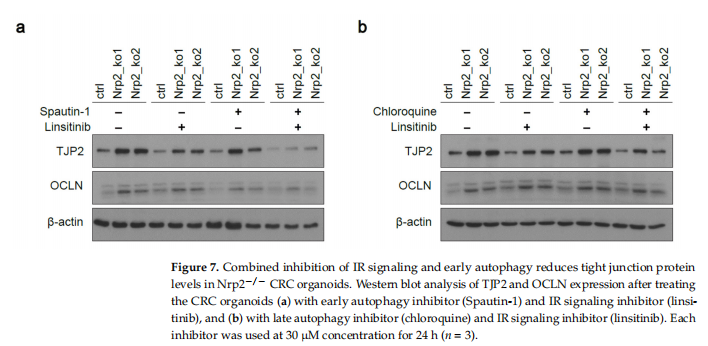
(图七)
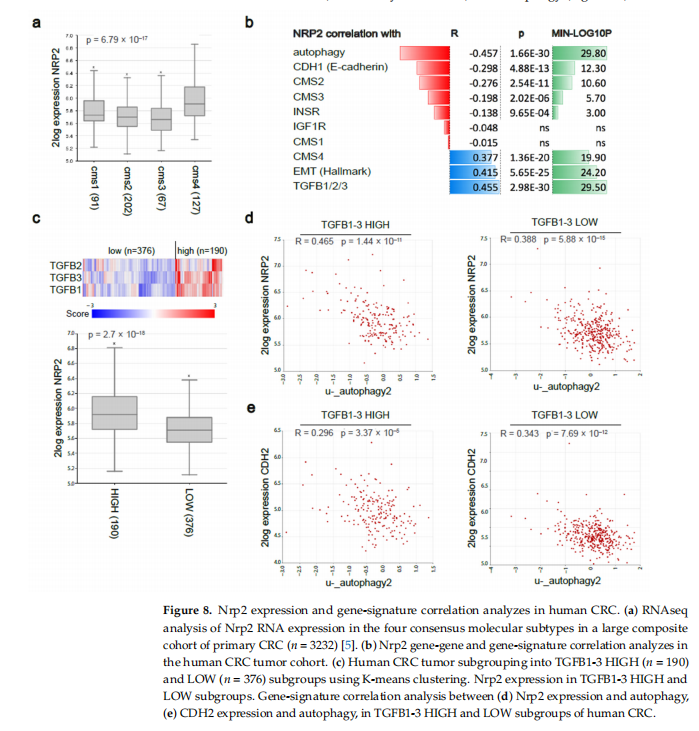
(图八)
结论
本研究利用小鼠间充质样CRC类器官诱导CRISPR-Cas9介导的Nrp2敲除。Nrp2耗竭导致CRC类器官中侵袭性较小的表型,MET和细胞-细胞连接稳定证明了这一点。此外,转录组分析和信号通路分析揭示了Nrp2敲除类器官对生存机制的从头获得依赖性,例如IR信号传导和自噬。值得注意的是,Nrp2敲除后CRC类器官中获得的表型在皮下肿瘤中得到保留,并在人类CRC肿瘤中得到扩展。
肿瘤衍生的类器官具有初始癌组织的遗传异质性和表型特征。因此,从CRC进展的不同阶段建立的具有不同突变和表型特征的类器官模型可以作为研究治疗方式的潜在机制和细胞毒性作用的稳健模型。
文章出自:细胞实验外包 想了解更多请关注:http://www.do-gene.com/




